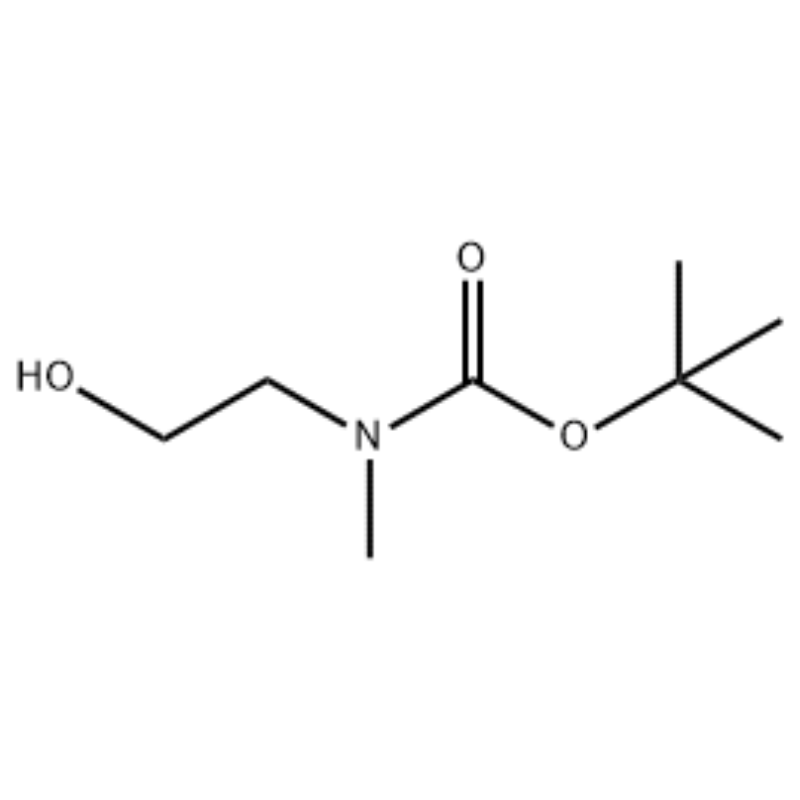
Zu enger Léisung vun 2-(Methylamino)ethanol (500 mg, 0,53 ml, 6,66 mmol) an CH2Cl2 (20 ml) gouf Boc2O (1,48 g, 6,79 mmol) bäigefüügt, gefollegt vum Rühren bei Raumtemperatur fir 1 Stonn.D'Reaktiounsléisung gouf mat Salzlake a CH2Cl2 extrahéiert.Déi organesch Schicht sou kritt gouf iwwer MgSO4 gedréchent a gefiltert.Duerno gouf de Filtrat am Vakuo konzentréiert fir d'Objetverbindung ze kréien (faarweg Ueleg, quantitativ);1H NMR (200 MHz, CDCl3) delta 3,74 (q, J= 10,5, 5,2 Hz, 2H) 3,25 (t, J= 5,2 Hz, 2H) 2,91 (s, 3H) 1,45 (s, 9H);Massespektrum m/e (relativ Intensitéit) 144 (20) 102 (24) 57 (70) 44 (100).
Beispill 38;N1-(3-fluor-4-(2-(1-(2-(methylamino)ethyl)-1H-imidazol-4-yl)thieno[3,2-b]pyridin-7-yloxy)phenyl)-N3 -(2-methoxyphenyl)malonamid (96);Schrëtt 1: tert-Butyl-2-Hydroxyethyl(Methyl)carbamate (97) (J. Med. Chem., 1999, 42, 11, 2008) Zu enger Léisung vun 2-(Methylamino)ethanol (5,0 g, 67 mmol) an THF (50 ml) bei RT gouf bäigefüügt Boc2O (15,7 g, 72 mmol) an d'Reaktiounsmëschung gouf bei RT fir 4 Stonnen gerührt.D'Reaktiounsmëschung gouf bis dréchent konzentréiert an d'Titelverbindung 97 gouf direkt an de nächste Schrëtt benotzt ouni zousätzlech Reinigung (11,74 g, 100% Ausbezuele).MS (m/z): 176,2 (M+H).
Virbereedung vu l-2-[4-Brom-2-(4-oxo-2-ftiotaioxo1hiazolidin-5-ylidenmefliyl)phenoxy]efliyl-3-efliyl-l-methylurea (Compoiotamd 161) Schrëtt 1: Synthese vun t-butyl2- Hydroxyethylmethylcarbamat;Zu enger Léisung vun 2-(Methylamino)ethanol (500 mg, 0,53 ml, 6,66 mmol) an CH2Cl2 (20 ml) gouf BoC2O (1,48 g, 6,79 mmol) dobäigesat, gefollegt vum Rühren bei Raumtemperatur fir 1 Stonn.D'Reaktiounsléisung gouf mat Salzlake a CH2Cl2 extrahéiert.Déi organesch Schicht sou kritt gouf iwwer MgSO4 gedréchent a gefiltert.Duerno gouf de Filtrat ënner Vakuo konzentréiert fir d'Objetverbindung (faarweg Ueleg, quantitativ) ze kréien; 2H) 2,91 (s, 3H) 1,45 (s, 9H);Massespektrum m/e (relativ Intensitéit) 144 (20) 102 (24) 57 (70) 44 (100).
2-(Methylamino)ethanol (90,1 g, 1,2 mol) gouf an 1,2 L Methylenchlorid opgeléist, a BoC2O (218 g, 1 mol) gouf lues a lues derbäi bäigefüügt, beim Rühren bei 00C, gefollegt vun 3 Stonnen bei Raumtemperatur.D'Reaktiounsmëschung gouf sequenziell mat 700 ml vun enger wässerlecher Léisung vu gesättigte Ammoniumchlorid an 300 ml Waasser gewascht.Déi gewascht Mëschung gouf dehydréiert mat waasserfräiem Natriumsulfat an konzentréiert ënner engem reduzéierten Drock, fir d'Verbindung (a) (175 g, 1 mol, 100%) als Ueleg ouni Faarf ze kréien.TLC: Rf = 0,5 (50% EtOAc an Hex) visualiséiert mat Ce-Mo stain1H NMR (600MHz, CDCl3) Delta 1,47 (s, 9H), 2,88 (br s, IH), 3,41 (br s, 2H), 3,76 (br s, 2H).
90,1 g (1,2 mol) 2-(Methylamino) Ethanol gouf an 1,2 L Methylenchlorid opgeléist, 218 g (1 mol) Boc2O goufe lues derbäi bäigefüügt, während déi resultéierend Léisung bei 0C gerührt gouf, an déi resultéierend Léisung gouf bei 0C gerührt. Raumtemperatur fir 3 Stonnen.D'Reaktiounsmëschung gouf sequenziell mat 700 ml vun enger wässerlecher gesättigter Ammoniumchlorid-Léisung an 300 ml Waasser gewäsch, dehydréiert mat waasserfräiem Natriumsulfat, an dann ënner reduzéierter Drock konzentréiert fir 175 g (1 mol) vun enger achromescher Uelegverbindung ze kréien, geschützt vum Boc Grupp (Ausbezuelen: 100%).[0140] 1H NMR (600MHz, CDCl3) delta 7.84 (br s, 2H), 7.76 (br s, 2H), 4.34 (d, J = 15.0 Hz, 2H), 3.63 (br s, 2H), 3.04 (d) , J = 15,0 Hz, 3H), 1,46 (d, J = 16,2 Hz, 9H) [0141] 90 g (0,514 mol) vun der kritt Verbindung gouf an 1,5 L vun tetrahydrofuran opgeléist, 88,0 g (539 mol) vun N- Hydroxyphthalimid an 141 g (0,539 mol) Triphenylphosphin goufen dozou bäigefüügt, 106 ml (0,539 mol) Diisopropylazodicarboxylat goufe lues a lues derbäi bäigefüügt, wärend déi resultéierend Léisung bei 0C rührt, an déi resultéierend Léisung gouf fir 3 Stonnen gerührt, während d'Temperatur dovun eropgeet. op Raumtemperatur.No der Konzentratioun vun der Reaktiounsmëschung ënner reduzéierter Drock, gouf 600 ml Isopropylether dozou bäigefüügt, déi resultéierend Léisung gouf bei 0C fir 1 Stonn gerührt, a wäiss festen Typ Triphenylphosphinoxid gouf gefiltert.De Feststoff gouf mat 200 ml Isopropylether ofgekillt op 0C gewäsch a mam éischte Filtrat gesammelt, an dat resultéierend Filtrat gouf ënner reduzéierten Drock konzentréiert fir 198 g vun enger Mëschung aus Compound XX an Diisopropylhydrazodicarboxylat an engem Mëschverhältnis vun 10 bis 15% ze kréien. (Ausbezuelen: 120%).1H NMR (600MHz, CDCl3) delta 7.84 (br s, 2H), 7.76 (br s, 2H), 4.34 (d, J = 15.0 Hz, 2H), 3.63 (br s, 2H), 3.04 (d) , J = 15,0 Hz, 3H), 1,46 (d, J = 16,2 Hz, 9H)
 Gebai 12, No.309, South 2nd Road, wirtschaftlech Entwécklung Zone, Longquanyi Distrikter, Chengdu, Sichuan, China.
Gebai 12, No.309, South 2nd Road, wirtschaftlech Entwécklung Zone, Longquanyi Distrikter, Chengdu, Sichuan, China. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404



















.png)


